Contoh Soal Teori Kinetik Gas Beserta Kunci Jawaban Lengkap – Ketika kamu belajar fisika di sekolah, akan bertemu dengan materi teori kinetik gas. Materi ini sering keluar ketika ulangan, untuk itu kamu harus memahaminya dengan baik.
Salah satu caranya dengan belajar mengerjakan soal-soal yang berkaitan dengan teori kinetik gas. Seringkali, soal yang telah kamu kerjakan juga akan muncul pada saat ulangan.
Pengertian Teori Kinetik Gas
Teori Kinetik Gas adalah suatu teori fisika yang menjelaskan perilaku gas berdasarkan sifat-sifat partikel-partikel gas. Teori ini mengasumsikan bahwa gas terdiri dari partikel-partikel yang bergerak secara acak dengan kecepatan yang berbeda-beda.
Berdasarkan teori kinetik gas, sifat-sifat gas seperti tekanan, volume, dan suhu dapat dijelaskan sebagai hasil dari gerakan partikel-partikel gas tersebut.
Teori kinetik gas didasarkan pada beberapa asumsi dasar, yaitu:
- Gas terdiri dari partikel-partikel kecil yang saling bergerak dengan kecepatan yang berbeda-beda.
- Partikel-partikel gas bersifat elastis, artinya mereka dapat saling bertumbukan dan memantul satu sama lain.
- Partikel-partikel gas memiliki volume yang sangat kecil dibandingkan dengan volume gas secara keseluruhan.
- Tidak terdapat gaya tarik-menarik antara partikel-partikel gas kecuali saat mereka saling bertumbukan.
Contoh Soal Teori Kinetik Gas Beserta Kunci Jawaban Lengkap
Berikut ini beberapa contoh soal teori kinetik gas yang sudah dilengkapi dengan kunci jawaban dan pembahasannya, yuk belajar sekarang.
1. Tekanan suatu gas yang volumenya 3 m3 yang berada dalam sebuah bejana tertutup (tidak bocor) dijaga tetap.
Suhu mutlak awalnya yakni 100 K, namun apabila volumenya dirubah menjadi 6 m3, maka hitunglah besar suhu mutlaknya!
Penyelesaian
Diketahui:
V1 = 3 m3
T1 = 100 K
V2 = 6 m3
Ditanyakan: 2 = ….?
Jawab:

Jadi suhu mutlaknya menjadi 200 K.
2. Suatu gas dengan volume 2 m3 berada dalam bejana tertutup (tidak bocor) yang suhunya dijaga tetap, tekanan mula-mula gas tersebut adalah 2 Pa. Jika tekanannya dinaikkan menjadi 4 Pa, tentukanlah besar volumenya?
Penyelesaian
Diketahui:
V1 = 2 m3
P1 = 2 Pa
P2 = 4 Pa
Ditanyakan: V2 = ….?
Jawab:
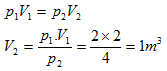
3. Sebanyak 40 L oksigen pada suhu 47° C dan tekanan 2,5 atm ditekan sehingga volumenya menjadi 20 L dan pada saat bersamaan suhu naik menjadi 127° C, tekanan yang diberikan tersebut adalah …
Penyelesaian
Diketahui:
V1 = 40 L = 0,04 m³
T1 = 47°C = 273 + 47 = 320 K
P1 = 2,5 atm
V2 = 20 L = 0,02 m³
T2 = 127°C = 273 + 127 = 400 K
Ditanya: P2 = …?
Jawab:

Jadi tekanan yang diberikan pada keadaan akhir sebesar 6,25 atm
4. Gas ideal terdapat di sebuah ruangan tertutup dengan volume V, tekanan P dan suhu T. Jika volumenya mengalami perubahan menjadi 1/2 kali semula dan suhunya meningkat menjadi 4 kali semula, maka tekanan gas yang berada dalam sistem tersebut adalah ?
Penyelesaian
Diketahui:
P1 = P
V1 = V
T1 = T
V2= 1/2V
T2 = 4T
Ditanya P2?
Jawab:

5. Suatu gas dengan volume 2 m3 terdapat dalam sebuah bejana tertutup (tidak bocor) dengan suhu yang dijaga tetap, pada tekanan mula-mula gas tersebut yakni 2 Pa.
Apabila tekanan gas dinaikkan menjadi 4 Pa, maka tentukanlah besar volume?
Penyelesaian
Diketahui:
V1 = 2 m3
P1 = 2 Pa
P2 = 4 Pa
Ditanyakan: V2 = ….?
Jawab:
P1V1 = P2V2
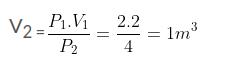
6. Tekanan suatu gas dengan volume 3 m3 yang berada dalam bejana tertutup (tidak bocor) dijaga tetap. Suhu mutlaknya mula-mula 100 K. Jika volumenya dirubah menjadi 6 m3, hitunglah besar suhu mutlaknya!
Penyelesaian:
Diketahui:
V1 = 3 m3
T1 = 100 K
V2 = 6 m3
Ditanyakan: 2 = ….?
Jawab:

7. Sebuah tangki diisi dengan 30 kg oksigen pada tekanan 2 × 105 Pa dan suhu 47° C. Tangki memiliki lubang kecil sehingga sejumlah gas dapat lolos keluar. Pada suatu hari, ketika suhu 27° C dan tekanan dalam tangki 1,5 × 105 Pa , maka massa oksigen yang lolos keluar dari tangki adalah …
Penyelesaian

9. Di dalam sebuah tabung yang tertutup, volume gas dapat berubah-ubah dengan tutup yang mampu bergerak, awalnya memiliki volume 1,2 lt. Pada saat itu tekanan telah diukur 1 atm dengan suhu 27O.Apabila tutup tabung ditekan sehingga tekanan gas yang dihasilkan menjadi 1,2 atm serta volume gas menjadi 1,1 lt. Berapakah suhu gas ini?
Penyelesaian
Diketahui:
V1 = 1,2 lt
P1 = 1 atm
T1 = 27O + 273 = 300 K
V2 = 1,1 lt
P2 = 1,2 atm
Ditanyakan: T2 =….?
Jawab:

10. Satu mol gas berada dalam tabung yang volumenya 50 liter. Bila suhu gas itu 227oC, berapa tekanan gas?
Penyelesaian
Diketahui:
n = 1 mol
V = 50 L = 5 . 10-2 m3
R = 8,31.103 J/kmol K
T = 227oC = (227 + 273) K = 500 K
Ditanyakan: p = ….?
Jawab:

Itulah beberapa contoh soal teori kinetik gas yang sudah dilengkapi dengan kunci jawaban. Kamu bisa belajar sendiri di rmah dengan memahami alur pengerjananya.

